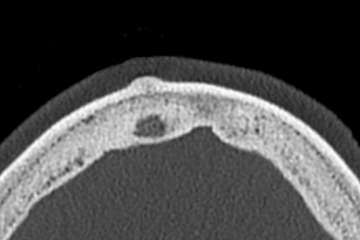
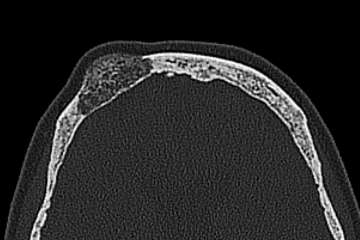
Zerebrale Metastasen machen bis zu 50% aller Hirntumore bei Erwachsenen aus. Ca. 15-30% aller Malignom Patienten entwickeln im Verlauf der fortschreitenden Erkrankung Hirnmetastasen. 90% aller Patienten mit Erstdiagnose einer Hirnmetastase haben auch weitere, extrakranielle Manifestationen der Metastasierung. Bei Patienten ohne bekanntes Malignom in der Vorgeschichte zeigen in ca. 15% aller Fälle die ersten Symtpome aufgrund der Hirnmetastase. Die metastatische Streuung erfolgt hauptsächlich auf hämatogenem Weg.
Epidemiologie
Metastasen sind die häufigsten Hirntumore bei Erwachsenen und machen knapp über 50% aller intrakraniellen Pathologien aus. Bei Kindern sind es nur ca. 6% aller Hirnpathologien. 15% aller Tumorpatienten entwickeln im Verlaufe der Erkrankung Hirnmetastasen. Die Metastase ist der häufigste Tumor bei Erwachsenen in der hinteren Schädelgrube (hämatogene Streuung über den Batson Plexus – klappenloses Venengeflecht). Bei supratentoriellen Metastasen treten 80% in den Hemisphären auf, meist an der Rinden-Mark Grenze und häufig postzentral an der Greze von Parietal-Temporal-und Frontallappen (whs. aufgrund des Endstromgebietes der A. cerebri media). Lungen- und Brust Karzinome machen >50% aller Hirnmetastasen aus.
Ätiologie von zerebralen Metastasen bei Erwachsenen:
| Primärtumor: | Prozentuale Anteile: |
| Lungen Ca | 44% |
| Brust Ca | 10% |
| Nierenzell Ca | 7% |
| G-I-Trakt | 6% |
| Melanome | 3-16% |
| Andere | 10% |
Klinik
Wie bei allen Hirntumoren treten neurologischen Defizite eher schleichend auf (Wochen – Monate) und nicht hoch akut wie bei vaskulären Ereignissen. Typische Symptome sind 1: Kopfschmerzen (in 50% der Fälle) mit Übelkeit und Erbrechen, 2: Fokal neurologische Defizite, 3: Epilepitsche Anfälle (15%) und 4: Persönlichkeitsveränderungen (Depression, Lethargie, Apathie, Verwirrtheit). CAVE: Akute Symptome können bei eingebluteten Metastasen auftreten.
Radiologische Befunde
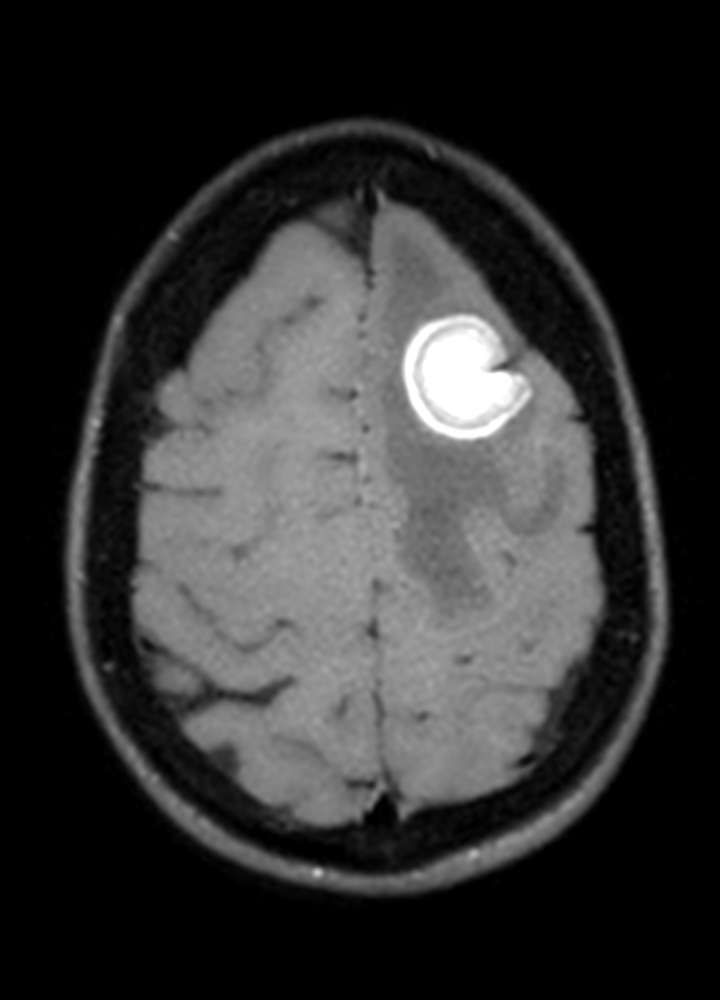
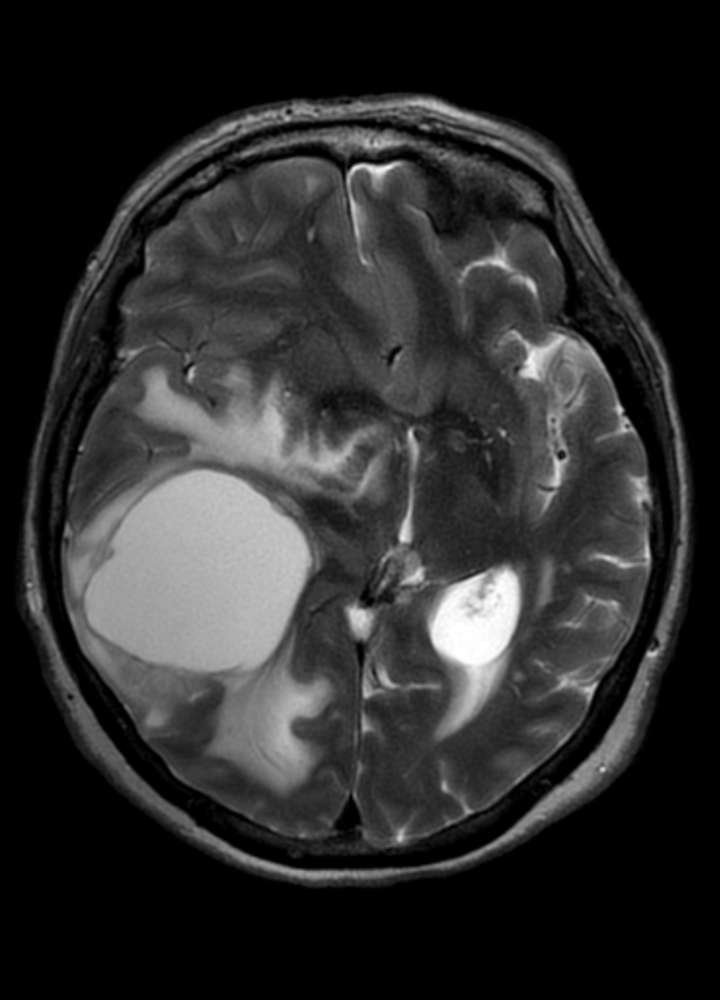
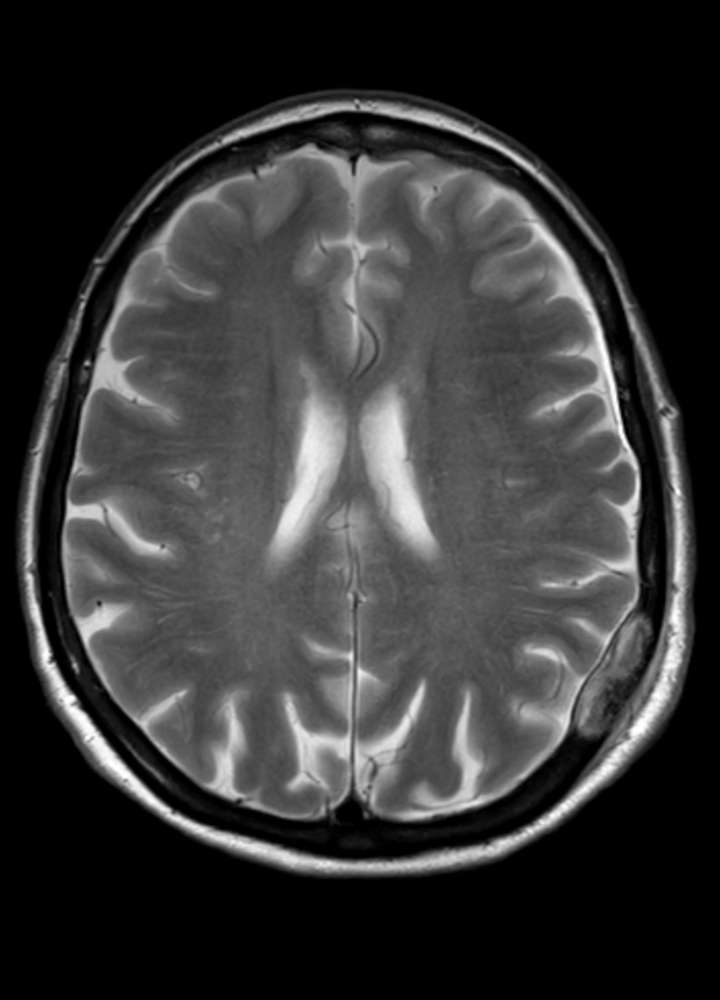
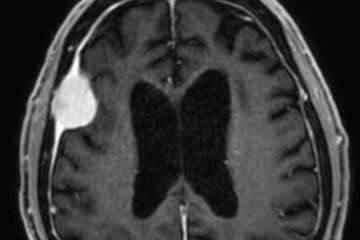
In der MR Bildgebung zeigen Metastasen alle möglichen Konfigurationen – sie können solide sein, zystisch, homogen oder heterogen. Selten sieht man Kalzifikationen. Typischerweise tendieren Lungen-Ca, Brust-Ca und GI-Trakt Ca zu Zystenbildungen. Metastasen zeigen ein Enhancement, dies kann nodulär sein oder nur am Rande der Raumforderung mit zentral nekrotischem oder eingeblutetem Zentrum. Typischerweise tendieren Melanome, Nierenzell-Ca, Brust-Ca, Lungen-Ca, Thyreoid-Ca, Retinoblastome und Choriocarcinome zu Einblutungen. Bei atypischen Einblutungen muss man neben Hirnmetastasen differentialdiagnostisch an vaskuläre Malformationen denken (z.B. Kavernome). Gegenüber Astrozytomen sind Metastasen eher besser zum Hirnparenchym abgegrenzt. Prostata-Ca und Brust-Ca (Oestrogen- und Progestereonrezeptoren positiv) zeigen eine höhere Rate an ossärer Metastasierung bevor das Hirnparenchym betroffen ist. Alle Metastasen zeigen ein miteinhergehendes Hirnödem.
Differentialdiagnosen
Primäres / sekundäres zerebrales Lymphom, Gliome, Meningeom (bei duraständigen Metastasen), eingeblutete occulte zerebrovaskuläre Malformationen (Bsp: Kavernom), Hirnabszess
Besonderes / zu beachten
Solitäre Metastasen:
Bei Erstmanifestation einer Hirnmetastase zeigen ca. 50% der Patienten eine solitäre Metastase in der CT-Bildgebung. Bei ergänzender MR-Bildgebung zeigen nur noch <30% einen solitären Herd. In ca. 1-3% der Fälle sind solitäre Metastasen im Hirnstamm zu finden.
Zunehmende Inzidenz von Hirnmetastasen:
Die verlängerte Überlebensdauer von Tumorpatienten aufgrund neuer systemischen Therapieansätzen könnte ein Grund für die Inzidenzzunahme von Hirnmetastasen sein. Zudem können mit den heute verfügbaren bilddiagnostischen Untersuchungen, Hirnmetastasen genauer dargestellt werden. Des Weiteren wird vermutet, dass bei systemischen Chemotherapien eine passagere Schwächung der Blut-Hirn-Schranke erfolgen kann und die zerebrale Streuung so einfacher erfolgt. Leider sind viele der heute angewendeten Chemotherapeutika nicht in der Lage die Blut-Hirn-Schranke zu durchdringen.
Small Cell Lung Cancer – SCLC:
SCLC machen etwa 20% aller Lungenkarzinome aus (80% Adenokarzinome – NSCLC). Jedoch tendieren SCLC häufiger zur zerebralen Metastasierung. 80% aller SCLC Patienten, welche >2 Jahre überleben, zeigen Hirnmetastasen. Die Therapie beinhaltet RTX und Chemotherapie, da diese Tumorart sehr strahlensensibel ist. Eine chirurgische Resektion einer SCLC-Hirnmetastase ist nur indiziert bei lebensbedrohlichen, grossen Läsionen oder bei lokalen Rezidiven nach Bestrahlung.
Non Small Cell Lung Cancer – NSCLC:
Die Prognose ist tendentiell besser als bei SCLC. Aufgrund der moderaten Resistenz auf eine Bestrahlung ist die chirurgische Resektion hier die Therapie der Wahl.
Melanome:
Typischerweise zeigen sich symptomatische zerebrale Metastasen von Melanomen ca. 14 Monate nach Erstdiagnose des Primarius. Das mediane Überleben bei nachgewiesener zerebraler Metastasierung beträgt ca. 6 Monate. Die chirurgische Resektion von 1-4 Metastasen ist indiziert, wenn diese komplett reseziert werden können und die systemische Progression nur langsam voranschreitet. Die Resektion von symptomatischen, lebensbedrohlichen Läsionen bei pancerebraler Metastasierung ist analog zu Metastasen von SCLC. Die Ganzhirnbestrahlung als palliative Therapie verlängert das Überleben um ca. 2-3 Monate. Die SRS wird bei Läsionen <3cm angewendet, welche nicht chirurgisch angegangen werden können und insgesamt nicht mehr als 4 Läsionen forhanden sind. Bei multiplen Metastasen ohne akute Lebensgefahr ist die Therapie der Wahl die Chemotherapie mit alkylierenden Medikamenten, Immunmodulatoren, BRAF-Inhibitoren und monoklonalen Antikörpern.
Strahlensensitivität von Hirnmetastasen:
| Strahlensensitivität: | Tumor: |
| hoch sensitiv | SCLC, Lymphom, Lekämie, Multiples Myelom, Keimzelltumore |
| moderat sensitiv | Brusttumore |
| moderat resistent | Kolon Ca, NSCLC |
| hoch resistent | Thyroidea, Nierenzell Ca, Malignes Melanom, Sarkom, Adenokarzinome |
Assoziierte Faktoren für eine bessere Prognose:
- Karnofsky Score > 70 Pte.
- Alter <60 Jahre
- Hirnmetastase ohne andere priphere Lokalisation
- Primärtumor unter systemischer Kontrolle
- >1 Jahr Überleben seit primärer Diagnose
- sinuläre oder wenige Hirnmetastasen
- weibliches Geschlecht
Operationsindikation
Bei unbekanntem Primarius sollte zur Diagnosesicherung eine stereotaktische Biopsie erfolgen, sofern die Metastase nicht chirurgisch vollkommen reseziert werden kann. Bei unkontrollierter peripherer Progression, stark verminderter Lebenserwartung und schlechtem klinischem Zustand (KPS <70), kann eine Biospie erfolgen mit palliativer Ganzhirnbestrahlung oder keiner Behandlung. Bei systemischer Kontrolle und KPS >70, sollte eine chirurgische Resektion angestrebt werden, sofern die Läsionen vollständig entfernt werden können (<4 Metastasen). Eine chirurgische Ausnahme bei pancerebraler Metastasierung (>4 Läsionen) stellt eine, aufgrund von Masseneffekt, lebensbedrohliche Situation oder schwerer klinischer Symptomatik dar. Eine radio-chemotherapeutische Nachbehandlung ist pflicht.
Indikation für die Operation:
für singuläre Läsionen:
- Systemische Kontrolle des Primarius
- Läsion chirurgisch komplett resezierbar
- Symptomatische oder lebensbedr. Läsion
- Läsion ist bestrahlungsresistent
- Rezidiv eines SCLC
- Unbekannter Pirumarius (Biopsie od. Resektion)
für multiple Läsionen:
- Eine Läsion ist symptomatisch oder lebensbedrohlich
- Alle Läsionen (<4) sind vollständig resezierbar
- Keine histologische Sicherung vorliegend (Biopsie od. Resektion)
Outcome
Mit optimaler Behandlung und einem Karnovsky > 70 ist das mediane Überleben über alle Gruppen von Hirnmetastasen berechnet bei ca. 26-32 Wochen (6-8 Monate). Unbehandelt liegt das mediane Überleben bei ca. 1 Monat nach Entwicklung von neurologischen Defiziten. Die Steroidtherapie verlängert das mediane Überleben auf 2 Monate. Eine Ganzhirnbestrahlung mit Steroidtherapie zeigt ein medianes Überleben von 3-6 Monaten. Patienten mit einer solitären Hirnmetastase und fehlenden Hinweisen für eine aktive systemische Progression haben das beste Überleben. Patienten mit kompletter chirurgischer Resektion von solitären Metastasen mit einer anschliessenden Ganzhirnbestrahlung haben ein medianes Überleben von ca. 40 Wochen (10 Monaten). 22% dieser Patienten haben jedoch innerhalb eines Jahres ein Rezidiv. Die Behandlung von Metastasen mit SRS inklusive einer Ganzhirnbestrahlung haben eine ähnliche lokale Tumorkontrollrate, jedoch eine unzuverlässige Rate der Grössenreduktion. Patienten mit multiplen Metastasen (<4), die vollständig entfernt wurden, haben ein ähnliches Überleben wie Patienten, mit Resektion einer singulären Metastase.